CHOQUE SEPTICO
El choque séptico o shock séptico es un estado anormal grave del organismo en el cual existe hipotensión prolongada por cierto período, generalmente dos horas o más, causada por una disminución de la perfusión tisular y el suministro de oxígeno como consecuencia de una infección y la sepsis que de ella resulta, aunque el microorganismo causal esté localizado por todo el cuerpo de manera sistémica o en un solo órgano, o sitio del cuerpo. Por lo general, requiere el uso de drogas vasoactivas para incrementar la presión arterial a pesar de haberse realizado una restauración adecuada de volumen corporal de la víctima.
Un choque séptico puede causar el síndrome de disfunción multiorgánica, conocida anteriormente como falla múltiorgánica, y la muerte. Sus víctimas más frecuentes son los niños, las personas inmunodeprimidas y los ancianos, ya que su sistema inmunitario no puede hacer frente a la infección de la forma más eficaz, como en los adultos sanos. La tasa de mortalidad por shock séptico es aproximadamente un 50%.
Unos de los microorganismos más comunes para la infección por choque séptico son los gramnegativos principalmente en el aparato genitourinario, es inducida por la mala instrumentación en los pacientes hospitalarios. Otros de los sitios más frecuente de los gramnegativos es el sistema respiratorio, seguido por el digestivo y las vías biliares.
En su fisiopatología nos dice que el mediador endógeno de la infección es la interlucina, los investigadores Beutler y sus colaboradores y de Tracey demostraron que la caquectina-TNF es un mediador central y proximal de la respuesta del huésped a la endotoxemia y bacteriemia.
La caquectina es una citocina que es secreta por macrófagos activados, es una proteína mediadora del factor de necrosis tumoral inducida por endotoxina.
Los estudios de Shires y sus colaboradores también hicieron investigación sobre el choque séptico en sus investigaciones menciona que hay una disfunción celular acompañada de una hemorragia la cual está asociada a la disminución del potencial transmembrana celular. Para que se de este mecanismo de potencial de membrana es necesario hablar del TNF-α humano porque es el mediador de la despolarización de la membrana de forma in vitro en el musculo esquelético.
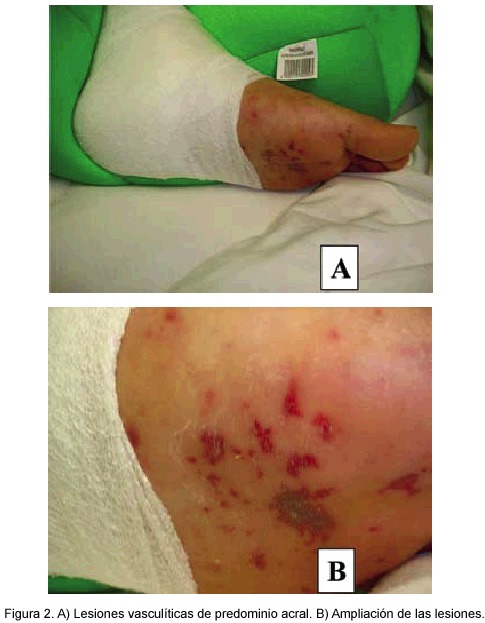
Dentro de las prioridades del choque séptico hay que tomar en cuenta las siguientes condiciones:
- Factores genéticos
- La Cascada inflamatoria
· Las citoquinas
· La respuesta inflamatoria
A continuación se hablara de estos factores más importantes dentro del mecanismo del choque séptico:
FACTORES GENÉTICOS
¿Por qué algunos individuos y no otros se infectan y sucumben por las graves complicaciones de la sepsis severa?
Existen datos suficientes como para pensar que tanto el riesgo de adquirir la infección como el riesgo de desarrollar complicaciones severas están determinados por factores genéticos del huésped. Estos incluyen defectos de genes únicos que afectan a receptores celulares; variantes genéticas que alteran la función de distintos mediadores inmunológicos, fisiológicos y metabólicos; o polimorfismos del ADN específicos de determinadas regiones génicas.
LA CASCADA INFLAMATORIA
En condiciones normales, cuando se produce una invasión microbiana del organismo, el sistema inmune pone en marcha una secuencia de acontecimientos denominada cascada inflamatoria.
LAS CITOQUINAS
La cascada inflamatoria se produce por la liberación de unos compuestos endógenos denominados citoquinas. Estos péptidos dan lugar a complejas reacciones inmunológicas que, en caso de superar los mecanismos naturales de control, pueden conducir al fallo multiorgánico y, potencialmente, a la muerte. Se han descrito 18 citoquinas con el nombre de interleukinas (IL), mientras que otras mantienen su descripción biológica original, como es el caso del factor de necrosis tumoral (TNF-α ). Algunas citoquinas favorecen la inflamación y se denominan proinflamatorias, como por ejemplo el TNF-α , la IL-1 y la IL-8; otras, inhiben la activación de las citoquinas proinflamatorias y se denominan antiinflamatorias, como la IL-6; y otras, como la IL-4, IL-10 y la IL-13, actúan indistintamente según los procesos biológicos. El interferón (INF-γ ) es otro ejemplo de esto último, aunque por lo general se tiende a considerarlo como proinflamatorio porque aumenta la actividad del TNF-α e induce la síntesis de óxido nitrico (NO).
LA RESPUESTA INFLAMATORIA
A pesar de la complejidad de la respuesta inmune inflamatoria, se puede elaborar un diagrama razonable de los hechos bioquímicos que se producen en la sepsis (gráfico 1). La presencia de microorganismos o de la endotoxina/lipopolisacaridasa (endotoxina/LPS), que es el componente polisacárido de la toxina bacteriana, además de activar al complemento, produce la activación de los macrófagos, los cuales sintetizan el TNF-α , el cual se une principalmente al pulmón, riñón e hígado, estimulando la producción en linfocitos, macrófagos y células endoteliales (aunque no sólo en ellos) de las interleukinas, el interferón, el factor estimulante de colonias de neutrófilos (FECN) y el factor activador plaquetario (PAF). El interferón y la IL-1 estimulan la síntesis y liberación endotelial de óxido nítrico. Todos estos mediadores mencionados, junto con el complemento activado, inducen la quimiotaxis de neutrófilos en los órganos diana (pulmón, hígado y riñón), dando lugar a su activación. La activación del complemento da lugar además a la degranulación de los mastocitos, liberándose histamina y serotonina, y a la activación del sistema kalikreína (K-K), con la producción de bradikinina. La activación de los neutrófilos tiene dos consecuencias: su degranulación, con la liberación de sus enzimas proteolíticos y la producción de radicales libre de oxígeno,estos últimos originan la peroxidación de los fosfolípidos de la membrana celular, cuya consecuencia es la producción de leukotrienos y prostanoides, estación última de la cascada inflamatoria.
Todos estos mediadores inflamatorios, debido a sus acciones son causa de las disfunciones orgánicas que caracterizan el cuadro clínico descrito del shock séptico.
Disfunción termorreguladora.
Debida fundamentalmente a las interleukinas, especialmente la IL-1 y la IL-6, al TxA2, la PGE2 y la prostaciclina.
Disfunción respiratoria
La taquipnea y la hiperventilación se deben al TxA2, la PGE2 y la prostaciclina. El aumento de la permeabilidad alveolocapilar está producida por el TNF-α , la IL-1, la IL-8, el PAF, las fracciones activadas del complemento C3a y C5a, la bradikinina, la histamina, la serotonina, la β -glucuronidasa, la elastasa, los leucotrienos LTB4 y LTC4 y el TxA2. La histamina, los leucotrienos LTC4, LTD4 y LTE4, la PGF2 y el TxA2 originan un incremento de la resistencia de la vía aérea El aumento de la permeabilidad alveolocapilar es el causante del edema pulmonar alveolointersticial y lesión pulmonar aguda, origen de la disminución de la compliance pulmonar y de la hipoxemia a pesar de la taquipnea refleja.
Disfunción cardiovascular
La taquicardia obedece a la PGE2, a la prostaciclina y al TxA2, además de respuesta refleja ante la hipotensión por la vasodilatación producida por el TNF-α , el PAF, la bradikinina, la histamina, la serotonina, los leucotrienos y la PGE2. Por otro lado, la hipotensión se debe también a la caída del gasto cardíaco originada por el PAF y por factores depresores miocárdicos entre los que están el NO, el TNF-α , la IL-1 y la IL-6.
La alteración del flujo coronario, consecuencia de la vasoconstricción coronaria de los leucotrienos y de la vasodilatación coronaria mediada por los factores mencionados anteriormente y especialmente por la prostaciclina, juega también un papel importante en la disfunción miocárdica.
En el territorio pulmonar, la hipertensión obedece a tres causas: a la vasoconstricción hipóxica pulmonar; a la contracción del músculo liso vascular producida por el TxA2 y las fracciones del complemento C3a y C5a; y a la agregación plaquetaria en los capilares pulmonares que da lugar a trombosis en los pequeños vasos, mediada por el TNF-α , la IL-1 y el PAF 4- Disfunción metabólica.
El NO inhibe la respiración mitocondrial, originando una alteración de la utilización tisular del oxígeno. La situación de shock, junto con las acciones del TxA2, la PGE2 y la prostaciclina, son los responsables de la acidosis láctica. A su vez, el TNF-α desencadena la liberación de las hormonas de stress (GH, ACTH y cortisol), dando lugar a la hiperglucemia de la fase inicial del shock séptico y la IL-1 estimula síntesis de ACTH, cortisol e insulina.
Disfunción renal, gastrointestinal y hepática
Tienen su origen además de en la hipoperfusión tisular, en la citotoxicidad del NO y en la citolisis producida por la activación del complemento y en el edema intersticial consecuencia del aumento de la permeabilidad capilar producida por el TNF-α , la IL-1, la IL-8, el PAF, las fracciones activadas del complemento C3a y C5a, la bradikinina, los leucotrienos LTB4 y LTC4 y el TxA2 . Por otro lado, el sistema reticuloendotelial del hígado actúa como filtro mecánico e inmunológico de la sangre portal, pero en la sepsis suele estar disfuncionante; la consecuencia es el paso de neutrófilos y citoquinas a través de la microcirculación hepática hacia la circulación sistémica, dando lugar a la adhesión, acumulación y degranulación de neutrófilos en los órganos diana y a la potenciación de la respuesta sistémica inflamatoria.
Disfunción hematológica
La IL-1 y el FECN estimulan la liberación de neutrófilos de la médula ósea dando lugar a la leucocitosis y desviación izquierda. Por otra parte, la acumulación de los neutrófilos en los órganos diana con la consiguiente activación y degranulación, sería la responsable de la leucopenia. Esta adhesión de neutrófilos está mediada por el TNF-α , por la unión de las fracciones activadas del complemento con sus receptores a nivel celular, por la IL-1, IL-8 y el PAF. Además, la IL-1 estimula la producción de linfocitos.
Las alteraciones de la coagulación en la sepsis (activación de la coagulación, depresión de los mecanismos inhibitorios de la coagulación e inhibición del sistema fibrinolítico) están mediados por el TNF-α , la IL-1, la IL-6, el PAF y la activación del complemento.
Disfunción del SNC
Aunque existen datos que sugieren que las citoquinas proinflamatorias suprimen directamente la función del SNC, los efectos acumulativos de la hipotensión y la hipoxemia suelen ser los responsables de los cambios en el estatus mental, especialmente en el anciano.




No hay comentarios:
Publicar un comentario